Diyabetik Anne Bebeği
1980'lerde David Barker ve meslektaşları, kardiyovasküler ve metabolik hastalıkların ana nedenlerinin köklerinin erken gelişimde olduğunu öne sürdüler. Artık hiperglisemik intrauterin ortamın yalnızca fetüs ve yenidoğanda kısa süreli önemli morbiditeden değil, aynı zamanda yetişkinlikte diyabet ve diğer kronik, bulaşıcı olmayan hastalıklara yakalanma riskindeki artıştan da sorumlu olduğuna dair güçlü kanıtlar vardır.
Gestasyonel diyabet (GDM) insidansı, obezite ve tip 2 diyabetin (T2D) yanı sıra gelişmekte olan ve gelişmekte olan ülkelerde de yüksek gelirli ülkelerde gözlenen salgın bağlamında dramatik bir şekilde artmaktadır.
Fetal aşırı beslenme: makrozomi
Fetal aşırı beslenmenin sonucu makrozomidir . Hamilelik sırasında fetüsü aşırı besin maddelerine maruz bırakan ana koşullar annede diyabet ve obezitenin yanı sıra aşırı gebelik kilo alımıdır (GWG). Anne obezitesi GDM veya önceden var olan T2D ile sıkı bir şekilde bağlantılıdır. GDM riski, normal kilolu hamile kadınlara kıyasla aşırı kilolu hamile kadınlarda 2,14 kat, obez hamile kadınlarda 3,56 kat ve aşırı obez hamile kadınlarda 8,56 kat daha yüksektir.
Maternal diyabet ve obezitenin fetal ve neonatal fizyoloji üzerindeki etkisinin mekanizmaları hala tam olarak anlaşılamamıştır. Pedersen'in 50 yıldan fazla bir süre önce formüle edilen hipotezi, fetal aşırı büyümenin, fetal pankreatik beta hücreleri tarafından insülin salınımını uyaran, anneden gelen glikozun artan transplasental transferiyle ilişkili olduğunu öne sürdü. İnsülin önemli bir fetal büyüme faktörü olduğundan , bunu takiben makrozomi ortaya çıkar. GDM'de hipergliseminin yanı sıra annenin metabolik ortamı insülin direnci (IR) ve inflamasyonla karakterizedir. Her iki durum da plasental besinlerin fetüse ulaşmasını artırır; yalnızca glikoz değil aynı zamanda amino asitler ve serbest yağ asitleri de vardır ve fetal büyümeyi etkiler. IR, fetusun substrat kullanılabilirliğini artıran anne hipertrigliseridemisini kolaylaştırır.
Aşırı fetal büyüme kavramı ya “makrozomi” kelimesiyle ya da “gestasyonel yaşa göre büyük” (LGA) ifadesiyle ifade edilir. Çalışmaya bağlı olarak, makrozomiyi tanımlamak için farklı eşik değerler önerilmiştir: 4000 ila 4500 g arasında bir BW veya >3500 g veya gebelik yaşına göre 90. yüzdelik dilimin (GA) üzerinde. LGA terimi GA için BW ≥ 90. yüzdelik veya > +2SD (>97. yüzdelik) anlamına gelir. Bu daha kesin tanım, doğumda GA'yı dikkate alır ve aşırı fetal büyümeye sahip prematüre yenidoğanların tanımlanmasına olanak tanır. Diyabetik annelerin yenidoğanlarında makrozomi, vücut yağında aşırılık, kas kütlesinde artış ve beyin boyutunda artış olmadan organomegali ile karakterizedir . Yenidoğanlarda vücut yağ yüzdesi , annenin glisemisi ve fetal insülin düzeyleri arasında doğrusal ve sürekli bir ilişki vardır.
Makrozomi, nedeni ne olursa olsun, asfiksi ve perinatal ölüm , doğum yaralanması, solunum sıkıntısı ve hipoglisemi gibi olumsuz perinatal sonuçlar için başlı başına bir risk faktörüdür. Bu riskler BW veya doğum yüzdeliği arttıkça artar. Makrozomik olmanın temel riski omuz distosisi ve sonrasındaki doğum yaralanmalarıdır. Bu son risk, vücut ağırlığı 4.500-4.999 g ve >5.000 g olan bebekler için en yüksek düzeydedir.
KISA VADELİ ETKİLER
Konjenital Malformasyonlar
Maternal diyabetin, özellikle de pregestasyonel diyabetin, konjenital anomalilerin görülme sıklığı üzerinde büyük sonuçları vardır.
Gebelik öncesi diyabetik annelerden doğan bebeklerin kardiyak malformasyonlara ( büyük arterlerin transpozisyonu , ventriküler veya atriyal septal defektler ve aort koarktasyonu), kaudal regresyon sendromuna , merkezi sinir sistemi kusurlarına (anensefali dahil nöral tüp defekti (NDT)) yakalanma olasılığı daha yüksektir. Mide-bağırsak malformasyonları (duodenal ve anal-rektal atrezi, hipoplastik sol kolon) ve iskelet ve genital-idrar yolu anomalileririskleri artar.
Maternal hiperglisemi, gelişen embriyoda çeşitli moleküler zincir reaksiyonlarını değiştirebilecek aşırı glukoz metabolizmasına neden olur:
1) hücre lipit metabolizmasında değişiklik, özellikle uteroda duktus arteriyozusun açıklığında rol oynayan prostaglandin E2 üretimi
2) yüksek glikoz seviyeleri , oksidatif strese (OS) neden olduğu ve sonrasında başta NDT olmak üzere fetal malformasyon riskini arttırdığı gösterilen reaktif oksijen türlerinin (ROS) aşırı üretimini indükler
3) yüksek glikoz, kaspaz ailelerinin üyeleri de dahil olmak üzere apoptotik hücre ölümünde rol oynayan birçok proteinin aktivasyonunu indükler.
Perinatal Ölüm
Her iki pregestasyonel diyabet türü de ölü doğum riskinin artmasıyla ilişkilidir . T1D'de bu tür risk çeşitli ülkelerde üç ila beş kat artmaktadır ve perinatal ölümlerin %75'inden fazlası konjenital anomalilere veya prematürite komplikasyonlarına bağlanmaktadır. T2D'de perinatal mortalite riski, T1D'den bile daha yüksek görünmektedir . Ölümler çoğunlukla ölü doğum, koryoamniyonit veya doğum asfiksisine bağlıdır. Sıkı bir glisemik kontrolün, TD1 ve TD2'li kadınlarda ölü doğum sayısını azalttığı gösterilmiştir. Ölü doğum riski, GDM'de, T1D ve T2D'ye göre daha az olmak üzere, hafifçe artabilir.
Hipertrofik Kardiyomiyopati
Maternal hiperglisemiye ve hiperinsülinizme maruz kalan fetüsler , hipertrofik kardiyomiyopati (çoğunlukla asemptomatik) geliştirmeye eğilimlidir. Miyokardiyopati öncelikle interventriküler septumu etkiler, ancak aort tıkanıklığının ciddiyetine ve kalp hipertrofisinin yaygınlığına bağlı olarak miyokarda da yayılabilir ve bazen ciddi morbidite ve mortaliteye neden olabilir .
Hem pregestasyonel diyabette hem de GDM'de miyokard hipertrofisi rapor edilmiştir. Diyabetik annelerden doğan bebeklerde %25 ila %75 arasında sıklıkta rapor edilmiştir. Pregestasyonel diyabet ile karşılaştırıldığında saf GDM'de görülme sıklığı daha düşüktür. En son çalışmalar, diyabetin türü ne olursa olsun, uygun bir annenin glisemik kontrolünün interventriküler septum hipertrofisini ve küçük fetal kalp fonksiyon bozukluğunu tamamen engellemediğini göstermiştir.
Rahim İçi Büyüme Kısıtlılığı ve Erken Eoğum
İntrauterin büyüme kısıtlaması, annedeki diyabetle daha az ilişkilidir, ancak ilerlemiş diyabetin ciddi vasküler komplikasyonları ve zayıf plasental perfüzyonu olan vakalarda rapor edilmiştir. Gebelik öncesi HbA1c ile doğumda azalmış fetal ağırlık arasında bir ilişki bulunmuştur. Hipotez, hamileliğin erken dönemindeki yüksek glikoz seviyelerinin, özellikle mikrovasküler hastalıklarla ilişkili olduğunda plasental gelişime zarar verdiği yönündedir . Plasental büyüme azalır ve plasenta fonksiyonları bozulur, bu da fetal büyümenin kısıtlanmasına neden olur.
Bu durum erken doğum riskini de beraberinde getirmektedir. Pregestasyonel diyabette prematüre doğum oranı %25'e kadar yükselir ve çoğunlukla geç preterm doğum (34-36. gebelik haftası (WG)) oluşur. T1D'de pregestasyonel hipertansiyon (HT) preterm doğumla ilişkiliyken, T2D'de üçüncü trimester glikozile hemoglobin (HbA1c) prematüritenin bir göstergesidir. GDM ve glikoz intoleransı, diğer diyabet komplikasyonlarından bağımsız olarak spontan erken doğum için risk faktörleridir, ortalama anne glikoz düzeyi ise erken doğum riskiyle ilişkilidir.
Yenidoğan Solunum Sıkıntısı Sendromu (RDS)
Diyabetik annelerin yenidoğanları , yenidoğan yoğun bakım ünitelerine kabulün önemli bir nedeni olan neonatal solunum sıkıntısı sendromu (RDS) açısından yüksek risk altındadır .
Bu komplikasyonun temel mekanizması, fetal hiperinsülinizm nedeniyle değişen akciğer yüzey aktif madde sentezine dayanır. İnsülinin doğum öncesi sürfaktan sentezini 34. haftadan sonra da değiştirdiği gösterilmiştir. İnsülin kortizolün sürfaktan sentezine olan katkısını antagonize etmekte ve bunu glukokortikoid reseptörlerini bloke ederek veya fosfolipid sentezinde rol oynayan enzimleri inhibe ederek yapmaktadır 36 ila 37 GA arasında RDS riskinin, özellikle pregestasyonel diyabet vakalarında daha yüksek olduğu gösterilmiştir. Bu nedenle, RDS ile ilişkili geç preterm doğum, intrauterin diyabet maruziyetinin özel bir özelliğidir ve bu bebekler , term bebeklere göre neonatal morbidite açısından daha fazla risk altındadır .
RDS'nin yanı sıra, diyabetik annelerden doğan bebekler , doğumda alveoler sıvının gecikmiş yeniden emilimi nedeniyle , özellikle sezaryen doğum bağlamında , yenidoğanda geçici taşipne riskinde artışa maruz kalır . Ayrıca, diyabetik gebelikten sonra artan perinatal asfiksi riskiyle birlikte mekonyum aspirasyonu riskinin arttığı da rapor edilmiştir. Bununla birlikte, bu tür komplikasyonlar esas olarak önceden var olan ciddi diyabetle komplike olan gebelikleri etkilemektedir.
Yenidoğan Hipoglisemisi
DAB'nde en sık görülen ve en önemli metabolik bozukluktur.
Başlıca hipoglisemi belirtileri, tremor, apne, laterji, emme güçlüğü, hipotoni, hipotermi, tiz ağlama, siyanoz ve konvülsiyondur. Görülme sıklığı, maternal glukoz kontrolüne, diabet süre ve şiddetine, kordon kanında glukoz, insülin, C-peptid ve HbAıc düzeyine bağlı olarak değişiklik gösterir. Neonatal hipoglisemide doğum sırasındaki maternal kan glukoz düzeyi de etkili olmaktadır. Nedeni, maternal glukoz desteğinden yoksun bebekte saptanan hiperinsülinizmdir. Henüz antiinsülin hormonları devreye girmemiştir, postnatal 2-4 saatlerde artması gereken glukagon düzeyi düşüktür. Serum noradrenalin düzeylerinde artış gözlenirken, kortikosteroid düzeylerinde değişiklik bulunmamıştır. Bu hormonların hipogliseminin kontregülasyonunda etkisiz kaldığı düşünülmektedir. Karaciğerden glukoz oluşumu azalmıştır. Hiperinsülinemiye bağlı olarak serbest immunoreaktif insülin düzeyi on kat, C-peptid immüno-raktivitesi ise üç kat artmıştır, proinsülin düzeyi de yüksektir. Plazma serbest yağ asitleri, Dbeta hidroksi bütirat; gliserol ve hepatik glukoz yapım oranında azalması, eksojen verilen intravenöz glukoz düzeylerinin hızlı düşüşü, hiperinsülineminin indirekt bulgularını oluşturur. Hipogliseminin her hastada belirtiye yol açmamasının nedeni belli değildir. Beyninde enerji için keton cisimlerin kullanılmasının ve artan glikojenin medulla ve spinal korda yayılarak santral sinir sistemine enerji kaynağının oluşturmasının bebeklerde daha çok asemptomatik seyir göstermesine yol açtığı düşünülmektedir.
Erken ve sık emzirme, bebeğin vücut ağırlığı ne olursa olsun, bağımsız olarak beslenebildiği sürece hipoglisemiyi önlemede anahtar olmaya devam etmektedir.
Yenidoğan Hipokalsemisi
Yenidoğanda serum kalsiyum düzeyinin 7 mg/dl veya iyonize kalsiyumun 3.5 mg/dl'nin altında bulunması ise hipomağnezemi olarak değerlendirmektedir. Hipokalsemi, gebelik yaşı ve maternal diabet kontrol derecesine bağlı olarak değişmektedir. % 15-30 oranında görülür ve sıklıkta birinci günün sonunda ortaya çıkar, genellikle belirti vermez. Hipomagnezemi ise % 30 olguda gözlenir, hipokalsemi ve hiperfosfatemi ile birlikte olabilir. Diabetli gebelerin son dönemlerinde yükselen serum kalsiyumunun bebekte fonksiyonel hipoparatroidiye yolaçtığı ve buna bağlı olarak hipokalseminin geliştiği ileri sürülmektedir. Gestasyonel diabette parathormonun azaldığı gösterilmiştir. Hipomagnezeminin ise direkt olarak parathormonunu süprese ettiği saptanmıştır. Doğum asfiksisine bağlı olarak gelişen hücre yıkımının yolaçtığı hiperfosfateminin de hipokalsemiyi arttırabileceği belirtilmektedir. Foton absorbsiyometrisi ile DAB'nde kemik mineral içeriğinin azaldığı gösterilmiştir.
Mekanizma hala belirsizdir ancak özellikle üçüncü trimesterde kalsemi ve D vitamini konsantrasyonlarının azalmasıyla birlikte hamilelik sırasında anormal bir kalsiyum fosfor metabolizmasını içeriyor gibi görünmektedir . Şiddeti annenin diyabet kontrolünün derecesi ile ilişkili olabilir. GDM gelişen kadınların D vitamini eksikliği yaşama olasılığının daha yüksek olduğuna dair kanıtlar giderek artmaktadır. Prematürite ve perinatal asfiksi gibi diğer faktörler düşük kalsiyum seviyelerine katkıda bulunabilir.
Yenidoğan Polisitemisi ve Hiperbilirubinemi
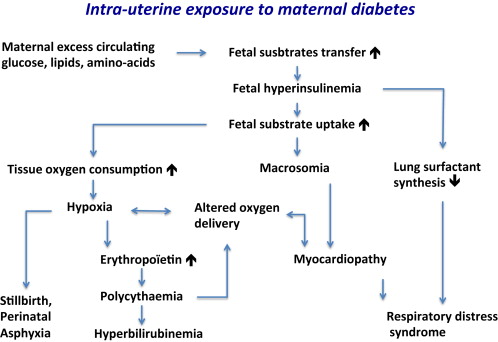
İnsülin kaynaklı yüksek glikoz alımına ve metabolizma hızına ikincil olarak göreceli fetal hipoksi , eritropoietin salgısının artmasına ve bunun sonucunda fetal kırmızı hücre üretiminin artmasına neden olur. Polisiteminin görülme sıklığı ve şiddeti, annenin kötü glisemik kontrolü ile ilişkilidir.
Diyabetik bir annenin bebeklerinde görülen normovolemik polisitemi kanda hiperviskoziteye neden olabilir. Erken semptomlar spesifik değildir: beslenme sorunları, aşırı görünüm, siyanoz , uyuşukluk, hipotoni , solunum sıkıntısı, gerginlik ve sinirlilik, nöbetler (çoklu serebral enfarktüs nedeniyle), nekrotizan enterokolit , hiperbilirubinemi ve hipogliseminin hepsinin ilişkili olduğu bulunmuştur. Diyabetik anne bebeklerinde böbrek trombozu ve diğer damar trombozları daha sık görülür.
Hiperbilirubinemi geleneksel olarak anne diyabetinin neonatal bir komplikasyonu olarak kabul edilir. Potansiyel olarak toksik seviyeler tedavi edilirse, ki bu genellikle böyledir, ciddi bir komplikasyon değildir. Tehlike , klasik olarak anne diyabeti vakalarında bildirilmeyen hiperbilirubinmik ensefalopati ve kernikterus riskindedir. Polisitemi, hiperbilirubineminin nedenlerinden biri olarak kabul edilir, ancak erken doğum, zayıf karaciğer konjugasyonu gibi ek mekanizmaların da söz konusu olması muhtemeldir.
UZUN VADELİ ETKİLER
Obezite ve T2D
Anne karnında diyabete maruz kalmanın çocuklukta aşırı kilo ve obezite ile T2D riski üzerindeki sonuçları Pima Kızılderililerinde yapılan çalışmalarla gösterilmiştir. Pima Kızılderililerinde genetik nedenlerden dolayı olağanüstü derecede yüksek obezite ve T2D prevalansı var. Pima kadınlarının çocuklarında T2D prevalansı, anneleri diyabetik veya prediyabetik olanlarda altı kata kadar artmaktadır ve çocukluk ve ergenlik dönemindeki diyabet neredeyse yalnızca diyabetik ve prediyabetik annelerin çocuklarında ortaya çıkmıştır. Aynı şekilde pregestasyonel T2D veya GDM'li annelerin çocukları doğumda ve her yaşta diyabetik olmayan annelerden doğanlara göre daha ağırdır. Diyabetik Pima kadınlarının çocuklarında diyabet ve obezite sıklığının yüksek olmasının yalnızca obezite ve diyabete genetik yatkınlıktan kaynaklanmadığına dair kanıtlar vardır.
Kardiyovasküler ve Böbrek Hastalıkları
Kontrollerle karşılaştırıldığında, anne diyabetine maruz kalan bebekler, olumsuz endotel bozulmasının biyobelirteçleri olan dolaşımdaki hücresel adezyon moleküllerinin artan seviyeleriyle birlikte daha kötü bir kardiyovasküler risk profiline sahiptir . Bu belirteçler ateroskleroz ve diyabetin en erken klinik öncesi evreleriyle ilişkilidir. Hamilelik sırasında diyabeti olan annelerin çocuklarında sistolik kan basıncı (SBP), hamilelik sonrasına kadar T2D gelişmemiş annelerin çocuklarına göre daha yüksekti: bu, yağlanmadan bağımsızdı.
Endotel disfonksiyonunun (ED), özellikle HT'de olmak üzere vasküler hastalıkların gelişiminde kritik öneme sahip olduğu düşünülmektedir. ED, vasküler tonus , inflamasyon ve OS ile ilgili düzenleyici fonksiyonların kaybıyla ve aynı zamanda bozulmuş vaskülogenez ve dolaşımdaki endotel progenitör hücrelerin aracılık ettiği onarım kapasitesiyle karakterize edilebilir. Diyabetik annelerden doğan bebekler, yaşamlarının ilerleyen dönemlerinde ED ve kardiyovasküler hastalıklar (CVD) geliştirmeye yatkındır.
Anjiyotensin II (AngII) endotelyal ve vasküler fonksiyonların bozulmasında da rol oynayabilir. Deneysel modeller AngII'nin endotelin-1'e yanıt olarak vazokonstriksiyonu arttırdığını ve insanda göbek venöz endotel hücrelerinde apoptozun indüklendiğini göstermiştir. GDM'li annelerin çocuklarında kordon kanındaki AngII konsantrasyonunda bir artış gözlemlenmiştir.
Diyabetik intrauterin ortama maruz kalma da böbrek hastalığı için güçlü bir risk faktörü olarak kabul edilmektedir. Diyabetik nefropati, son dönem böbrek hastalığının ana nedenidir. Pima Kızılderililerinde, diyabetik annelerin çocuklarında idrar albümin atılımında (BAE) artış gözlemlenmiştir: BAE, GDM'li annelerin çocuklarında %58, hamilelikten sonra diyabet gelişen annelerin çocuklarında %43 ve yavrularda yalnızca %40'tır. Bu fonksiyonel değişiklikler, muhtemelen nefron sayısının azalmasıyla ilgili benzer bir süreçle ilişkili olarak gelişen glomerüllerde hasara yol açabilir.
Mekanizmalar: oksidatif stresin rolü
Diyabetik anneden doğan çocuklarda kardiyometabolik hastalıkların gelişiminde rol oynayan olası faktörler arasında OS ve epigenetik değişiklikler öne sürülmüştür. Epigenetik faktörler bu sayımızın farklı bir bölümünde tartışılmaktadır.
Hiperglisemik bir ortam, özellikle serbest radikallerin aşırı üretimi ve radikal temizleyicilerin azalması olan GDM'li kadınlarda OS ile ilişkilidir. Hiperglisemi, poliol yolu , ileri glikasyon son ürünlerinin oluşumu , protein kinaz C'nin aktivasyonu , heksozamin yolu ve mitokondri tarafından artan ROS üretimi gibi çeşitli metabolik mekanizmalar yoluyla OS'yi indükler . Bu nedenle anne GDM'sinden kaynaklanan hiperglisemik intrauterin ortam fetüsü OS'ye maruz bıraktı. Aslında, GDM'li annelerden doğan bebeklerin kordon kanında malondialdehid düzeylerinde (lipit peroksidasyonunun son ürünü) bir artış ve süperoksit dismutaz (süperoksit anyon temizliğinden sorumlu enzim) aktivitesinde bir azalmadan bahsedilmiştir.
Kısaltılmış telomer uzunluğu, artan CVD, HT, obezite ve diyabet riskiyle ilişkilidir. İşletim sisteminin telomer yıpranmasında olası bir etkisi var gibi görünüyor. GDM'li kadınlardan doğan bebeklerde daha kısa telomer uzunluğunun gözlemlenmesi, kısalmış telomer uzunluğunun GDM'li çocukların yetişkinlik döneminde kardiyometabolik hastalık riskini artırabileceğini düşündürmektedir. AngII ayrıca, NO veya prostasiklin gibi endotel gevşetici faktörleri temizleyerek veya etkisiz hale getirerek ve güçlü bir daraltıcı olan peroksinitrit üreterek vasküler fonksiyonu etkileyebilen ROS seviyelerinin arttırılmasında da rol oynamaktadır. Bu nedenle AngII, GDM'li annelerin çocuklarında gözlenen endotel disfonksiyonuna ve daha sonra kan basıncında (KB) artışa neden olabilir.
Uzun vadeli sonuçlarda LGA olmanın sonucu
Bir dizi çalışma çocuklukta ve erken yetişkinlikte yüksek BW ile obezite arasında bir bağlantı olduğunu bildirmiştir. Bir meta-analiz, BW ≥ 4000 g'ın obezite riskini iki kat arttırdığını ve BW 90. persentil'i aştığında bu riskin yaklaşık 2.5 kat arttığını göstermiştir. LGA'nın (BW > 90. persentil) GDM veya anne obezitesiyle birlikte olması , çocukluk çağında metabolik sendrom (MS) riskini artırır.
Emzirmenin etkisi
Emzirmenin uzun süreli obezite üzerinde olumlu etkileri olduğu ileri sürülmüştür. Emzirmenin uzun vadeli avantajı, "doz-yanıt" etkisi ile de desteklendi. Daha uzun süreli emzirme, daha sonraki obeziteye daha düşük bir eğilimle ilişkilendirildi; her ay emzirme obezite riskinde %4'lük (%95 GA -6 - %2) bir azalma ile ilişkilendirilmiştir.
Emzirmenin olumlu etkisi, kısmen mamayla beslenen bebeklere kıyasla büyümenin daha yavaş olmasıyla ilişkilidir, çünkü doğum sonrası erken dönemde hızlandırılmış büyüme veya bebeklik döneminde doğum sonrası büyümenin hızla yakalanması, yetişkinlikte obezite ve KVH riskini artırır. Bununla birlikte, beslenmenin uzun vadeli sonuçları etkilediği kritik pencere dönemi iyi tanımlanmamıştır ve erken büyüme, ilk 2 WG'den yaşamın en azından ilk 2 yılına (ilk 1000 gün) kadar uzanan bir spektruma karşılık gelebilir. Yaşamın ilk haftasında daha fazla kilo alımının yetişkinlikte obeziteyi programlayabildiği gösterilmiştir: Bu dönemde mutlak kilo alımındaki her 100 gramlık artış, aşırı kilolu olma riskinde %28'lik bir artışla ilişkilendirilmiştir. eterli emzirme (≥6 ay), anne karnında diyabete maruz kaldıktan sonra çocukluk döneminde gözlemlenen yağlanma seviyelerindeki artışı da azaltır.
Kaynaklar:
https://www.sciencedirect.com/science/article/pii/S1521693414001631
https://www.perinataldergi.com/Files/Archive/tr-TR/Articles/PD-19930012013tr.pdf
